1. 탄화수소(HC)
- 탄소와 수소로 구성된 유기물로, C1~C4가 기체, C5~C15 액체, C16 이상은 고체
- 탄화수소는 포화탄화수소(C-C 단일결합)과 불포화탄화수소(C=C 이중결합, C≡C 삼중결합)로 나뉜다.
- 불포화탄화수소는 이중결합 또는 삼중결합을 갖고 있는 탄화수소이며 반응성이 커서 광화학반응이 활발
- 자연적인 발생량(탄광, 천연가스)이 많음, 인위적 발생량은 탄화수소 발생량 전체의 1% 정도
- 이중결합을 갖는 올레핀계 탄화수소는 대기 중에서의 반응성이 커서 광화학 스모그의 원인이 된다.
- 파라핀계 탄화수소는 NOx, SOx가 존재해도 에어로졸을 형성하지 않음.
- 메탄계 탄화수소의 지표부근 배경 농도는 약 1.5ppm
- 메탄계 탄화수소는 주로 미생물의 유기물 분해 작용에 의해 발생하며, 적외선의 특수파장을 흡수하여 온실기체로 작용한다.
- 메탄(CH4)은 천연가스의 원료이나 산소 부족시에는 질식성이 있는 가스이다.
참고) 탄화수소의 종류
| 파라핀계 | CnH2n+2 |
| 올레핀계 | CnH2n (불포화, 직렬쇄상 구조) |
| 나프텐계 | CnH2n (포화, 환상구조) |
| 방향족계 | CnH2n-6 (환상구조) |
| 아세틸렌계 | CnH2n-2 (삼중결합) |
(1) 파라핀계 탄화수소 (Paraffin Series, CnH2n+2)
- 직렬쇄상 구조(사슬모양 구조)이고, C-C 단일결합을 갖는 포화탄화수소 = 지방족 포화탄화수소
- CnH2n+2의 화학식을 가지며 n의 숫자에 따라 CH4(메테인), C2H6(에테인), C3H8(프로페인) 등
- 파라핀계의 명칭은 접미어로 -ane이 붙는다.
- 가지를 갖는 이소(iso) 화합물을 구조 이성질체로 갖는다.


(2) 올레핀계 탄화수소
- 직렬쇄상 구조(사슬모양 구조)이고, C=C 이중결합을 하나 갖는 포화탄화수소 = 지방족 불포화탄화수소
- CnH2n의 화학식을 가지며 C2H4(에틸렌), C3H6(프로필렌) 등이 있다.
- 이중결합을 가지고 있어 나프텐계, 방향족 탄화수소보다 대기 중에서 반응성이 크다.
- 광화학스모그에 적극 반응하여 촉매역할을 한다.
- 올레핀계의 명칭은 접미어로 -ene이 붙는다.


(3) 나프텐계 탄화수소 (Naphthene Series, CnH2n)
- 환상구조이고, C-C 단일결합을 갖는 포화탄화수소 = 지방족 고리 포화탄화수소
- CnH2n의 화학식을 가지며 n(≥3)의 숫자에 따라 C5H10(사이클로펜테인), C6H12(사이클로헥세인) 등
- 나프텐계의 명칭은 접두어로 Cyclo-가 붙는다.
- 일반적으로 파라핀계 탄화수소보다 융점이 낮고 액체를 이루는 것이 많다.
(4) 방향족계 탄화수소 (Aromatic series, CnH2n-6)
- 벤젠 고리를 포함하는 환상구조이고, C=C 이중결합을 갖는 불포화탄화수소
- CnH2n-6 (n≥6)의 화학식을 가지며 C6H6(벤젠), C7H8(톨루엔) 등이 있다.
- 냄새나 향기가 나는 방향족 탄화수소가 있다.
- 벤젠은 안정된 골격을 유지하는 특징이 있어 안정하다.
(4) - 1 단일방향족탄화수소 (MAH)
- 하나의 벤젠 고리로 이루어진 방향족 탄화수소
- 벤젠 고리를 중심으로 치환기가 붙어 있는 구조를 갖는다. 즉, 벤젠의 유도체
- 페놀, 톨루엔, 자일렌, 아닐린 등이 있다.
(4) - 2 다환방향족탄화수소 (PAH)
- 여러 개의 벤젠 고리로 이루어진 방향족 탄화수소
- 석유나 석탄에 포함, 유기물질의 불완전 연소로 배출됨
- 일부 종류는 발암성을 가지며, 돌연변이나 기형을 유발하는 경우도 있어서 오염물질로 분류되곤 한다.
- 비점과 융점이 높고 증기압이 낮으며, 물에 대한 낮은 용해도, 유기용매에는 높은 용해도
- 대부분 공기역학적 직경이 2.5㎛ 미만인 입자상, 가스상 물질
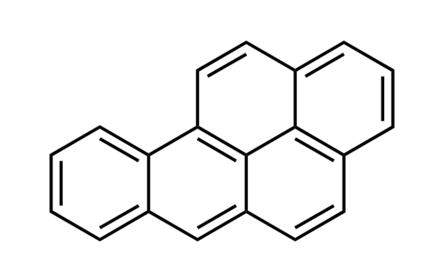
- 발암성 물질 예 : 벤조 [a] 피렌 (1군 발암물질, 불완전연소 과정에서 생성 ex) 담배연기, 배기가스, 쓰레기 소각연기 등)
(5) 할로겐 탄화수소 (HHC, Halogenated hydrocarbon)
- 탄화수소 화합물 중 수소가 할로겐으로 치환된 것으로 비인화성, 안정한 물질
- 독성은 화합물에 따라 차이가 있으나 다발성이며, 중독성이다.
- 대부분의 할로겐 탄화수소는 중추신경계 억제작용과 점막에 대한 자극효과를 가진다.
- 사염화탄소는 가열하면 포스겐이나 염소로 분해되며, 신장장애를 유발하고 간에 대한 독성이 심하다.
- 사염화에틸렌은 지방이 없는 한 소화관에서 흡수되기 어려우며, 사염화탄소보다 독성이 적다. 드라이클리닝 용제, 금속 세척제, 도료의 용제 등으로 이용
(6) 아세틸렌계 탄화수소 (Acetylene Series, CnH2n-2)
- 직렬쇄상 구조(사슬모양 구조)이고, C≡C 삼중결합을 갖는 불포화탄화수소
- CnH2n-2의 화학식을 가지며 C2H2(아세틸렌), C3H4(프로파인) 등이 있다.
- 올레핀계의 명칭은 접미어로 -yne이 붙는다.
'대기환경기사 필기 > 대기오염개론' 카테고리의 다른 글
| [대기오염개론] 실내오염물질 (0) | 2023.06.22 |
|---|---|
| [대기오염개론] 기타 가스상물질 (0) | 2023.06.21 |
| [대기오염개론] 일산화탄소(CO), 이산화탄소(CO2) (0) | 2023.06.19 |
| [대기오염개론] 질소산화물(NOx) (0) | 2023.06.19 |
| [대기오염개론] 황산화물(SOx) (0) | 2023.06.18 |

